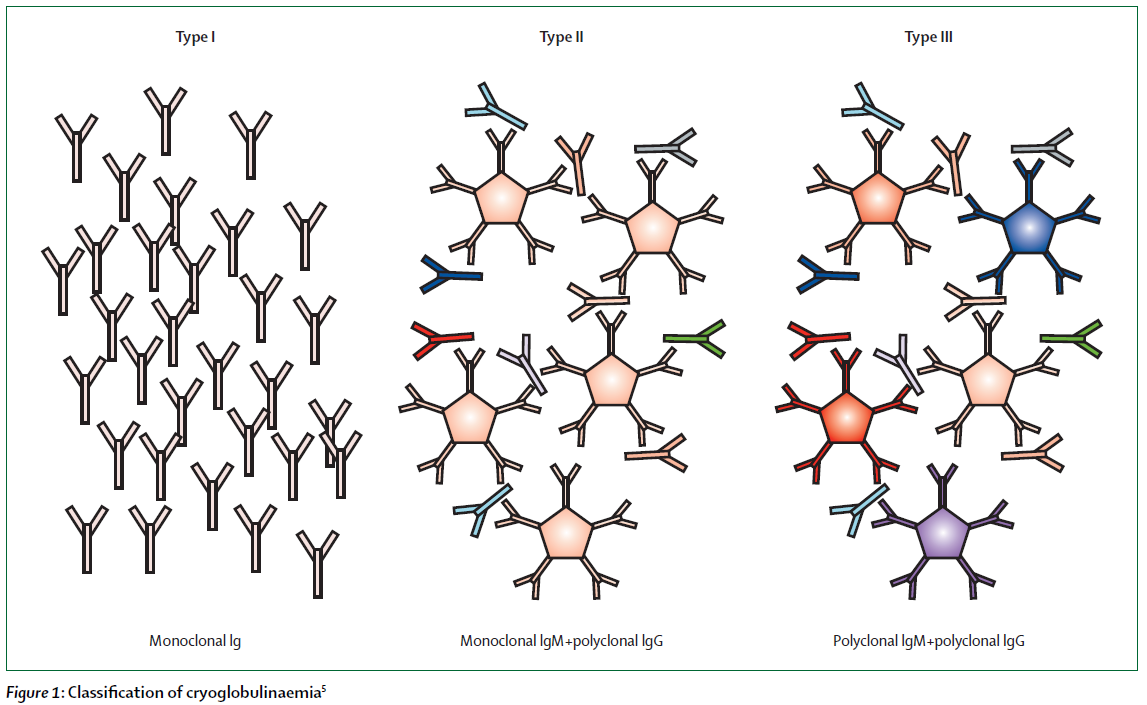
I型クリオグロブリン血症
Clinical presentation and outcomes of patients with type 1 monoclonal cryoglobulinemia.
Sidana S et al. Am J Hematol. 2017 Jul;92(7):668-673.
クリオグロブリン血症について、こちらもご覧ください。
・486名のクリオグロブリン血症患者の内、I型クリオグロブリン血症はクリオグロブリン血症全体の22%程度(II型は53%、III型は25%)
・診断時の平均年齢は59歳(31-91歳)
・54%が男性、95%がコーカサス地方出身者
・I型クリオグロブリン血症の内、IgG型は53%、IgM型が39%、IgGとIgMの混合は5%
・背景疾患は38%にMGUS(内64%がIgG型、31%がIgM型、IgGとIgMの混合は5%)、リンパ形質細胞性リンパ腫(LPL)は21%(内86%がワルデンストームマクログロブリン血症(IgM型)、9.5%がIgG型、4.8%がIgGとIgM型のLPLは4.8%)、MMは20%(内70%はくすぶり型)
《I型クリオグロブリン血症の臨床症状》

・皮膚所見(紫斑、潰瘍、壊疽、網状皮斑(Livedo reticularis))が多い
《I型クリオグロブリン血症の治療》

・治療は様々。背景のモノクローナルなリンパ増殖性疾患を意識する
《I型クリオグロブリン血症の予後》


・I型クリオグロブリン血症の平均生存期間は11.4年
強皮症腎クリーゼ Scleroderma renal crisis(SRC)
概念
・強皮症(Systemic Sclerosis: SSc)は血管障害や線維化によって皮膚硬化がや臓器障害が引き起こされることが特徴的な自己免疫性疾患(1)
・強皮症腎クリーゼ(Scleroderma renal crisis: SRC)は稀な強皮症の合併症(1)
・新規発症で急速進行性の腎動脈性高血圧、急速進行性乏尿性腎機能障害、中等度の血圧上昇と腎機能障害、正常血圧など様々な臨床スペクトラムを有する(1)
・SRCが強皮症の初期症状となることもあり得る(3)
・正常血圧SRCの1/4が強皮症の診断なく、SRCが初発症状となる(4)
疫学
・全強皮症では5-13%(1)
・びまん型では11-20%(1)(2)、限局型では4%(1)
・頻度はどんどん下がっていると(2)
・これはレイノー現象に対する血管拡張薬の使用が広がったためと、SRCのリスクとなるため、コルチコステロイドの使用が慎重となったためと考えられる(2)
・高血圧が主だが、正常血圧は10%に起こり、予後不良(2)
・溶血性微小血管障害は50%に起こる(2)
病態
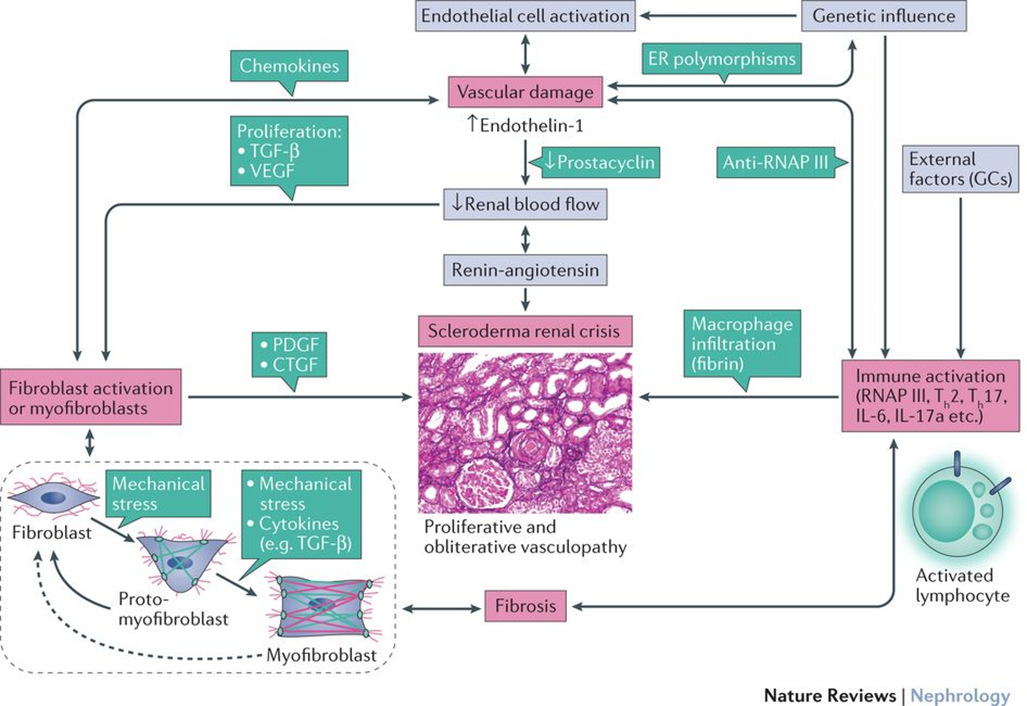
※下記表は文献(3)から

※下記表は文献(4)から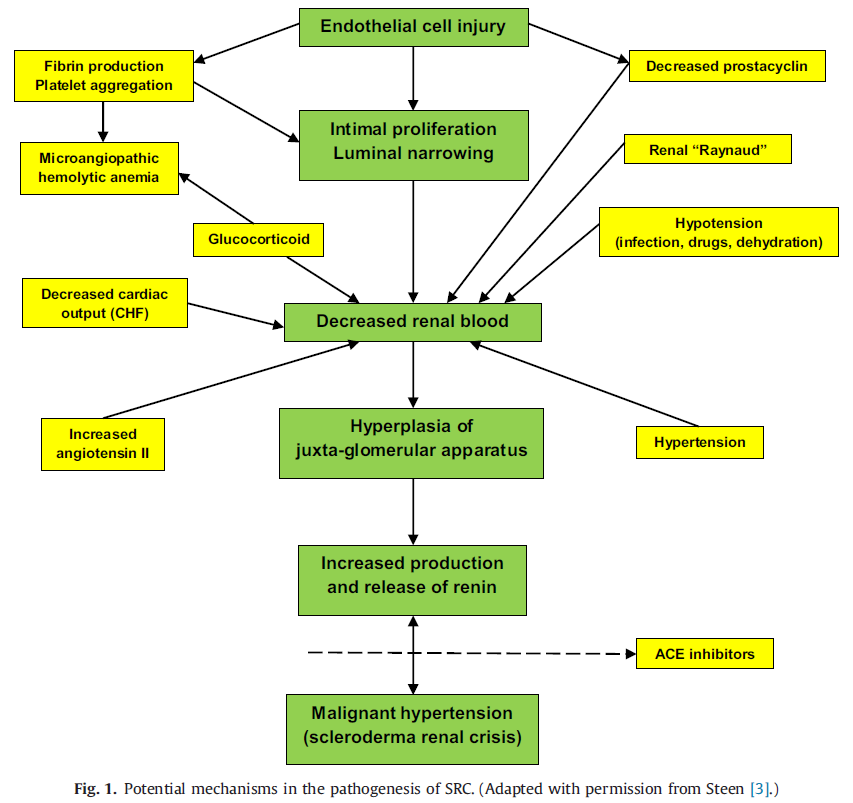
・明確に理解されているわけではないが、微小血管の内皮細胞障害が起こり、血管透過性が亢進することで内皮細胞の増殖、フィブリノイド血栓を伴う血小板凝集が起こる(2)
・これにより小葉間や球状腎動脈の内膜肥厚と線維化領域を伴う増殖性閉塞性血管症が起こる(Onion skin lesions)(2)
・腎血流が低下すると糸球体虚血が起こり、レニン-アンギオテンシン系が活性化し、重篤な腎動脈性高血圧を起こす(2)
・一方で狭窄した同部位では塞栓性微小血管障害や溶血性貧血が起こり、末梢血に破砕赤血球が出現する(2)
・この糸球体病変は非炎症性で免疫沈着物も認めない(2)
病理(3)
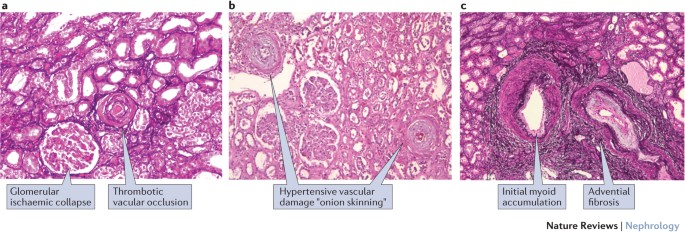

・a: 高血圧性血管障害, 血栓性血管閉塞, 糸球体の虚血性荒廃, びまん性尿細管変性
・b: Onion skin lesions
・c: 内膜の筋組織蓄積と外膜の線維化
リスク因子(1)
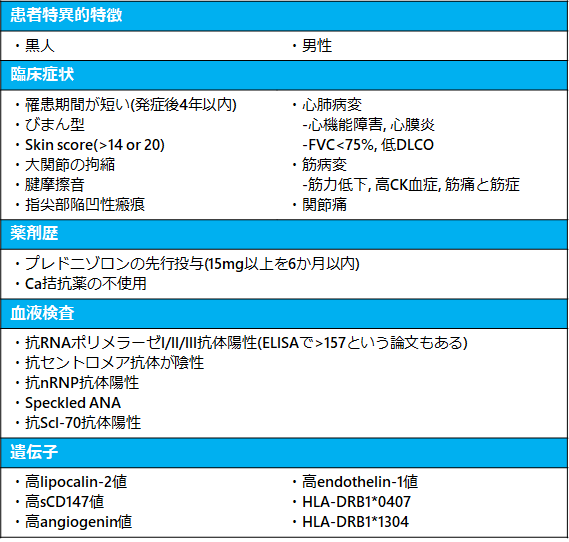
※sCD147: 細胞外マトリックスメタロプロテアーゼ阻害因子
・SRCの75%が強皮症発症(レイノー現象を除く症状)4年以内(2)
・1年間で急速に皮膚硬化が起こる場合もリスク(2)
・mRSSがSRC発症前の6か月間で、50%の患者で上昇したという(2)
・心拡大やうっ血性心不全は腎血流低下を起こし、SRCの潜在的なリスクとなり得る(2)
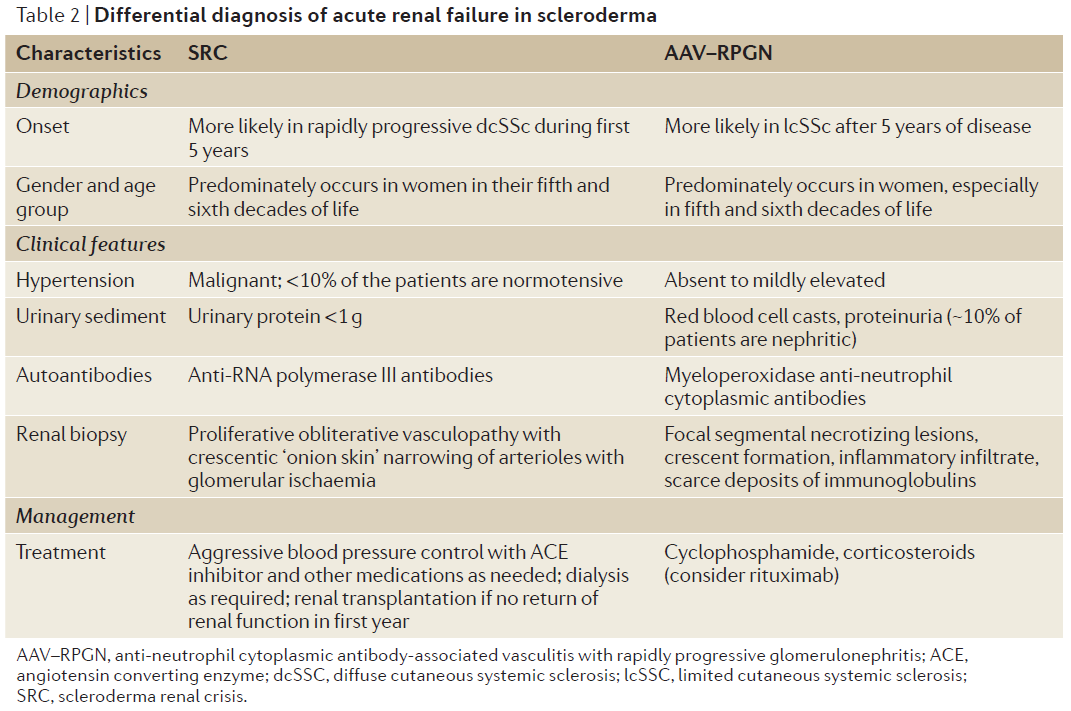
鑑別(1)
・ANCA関連糸球体腎炎(37%)
・TTP/HUS(21%)
・膜性腎症(7%)
・膜性増殖性糸球体腎炎(1%)
・その他の血管炎(結節性多発動脈炎、混合型クリオグロブリン血症、Goodpasture症候群)(7%)
・薬剤性腎症(D-ペニシラミン、シクロスポリンなど)(5%)
・シュウ酸腎症(4%)
・腎動脈狭窄(4%)
・腎前性(敗血症、脱水症)(1%)
ANCA関連糸球体腎炎
・特にMPO-ANCAが95%以上に見られる(1)
・pauci-immune壊死性、半月体形成性糸球体腎炎が腎生検で見られる(1)
・その他、肺胞出血や皮疹、手指虚血などの血管炎症状を認める(1)
・免疫抑制療法が有用なのはSRCと異なる(1)
・すべてのタイプのSSc(限局型から強皮症症状のないSScまで)に合併し(59%)(1)、抗Scl-70抗体陽性(77%)、SScの罹患期間が長い(8±7.7年)(1)
・正常血圧が多い(sBP<160mmHg)(82%)、MAHAやTTP、高レニン血漿を伴わない(1)
・別の報告ではRPGNを伴うAAVは限局型SScの晩期、Overlap症候群、稀に混合型クリオグロブリン血症に見られるという(3)
・診断が不明な時は腎生検を行う(3)
・無症状の時のANCA陽性は意味がない(SScでは0-11.7%でANCA陽性となる)(3)
※以下の図は論文(3)より引用
TTP
・抗ADAMTS-13抗体を伴うADAMTS-13活性の欠損、重篤な血小板減少(特に<5万/μl)、出血合併症(紫斑、消化管出血)、発熱、血漿交換が著効することなどはSRCよりもTTPを指示する所見(1)
・正常血圧が多く、限局型、長期罹患患者に多い(1)
・腎生検では原発性糸球体毛細血管の微小血管障害を認めるが、SRCでは糸球体外微小血管病変を有する点が異なる(1)
シュウ酸腎症
・脂肪吸収不良や抗菌薬が必要なSIBOを起こすほどの重篤な消化器病変を有する場合に疑う(1)
・正常血圧が多く、溶血や尿検査異常を伴わない(1)
・シュウ酸結晶は尿検査で認め、24時間蓄尿でシュウ酸の増加を認める(1)
・腎生検ではびまん性尿細管内の複屈曲性結晶を含むカルシウム沈着物を認める(1)
腎動脈狭窄
・ACE阻害薬を使用すると腎機能障害が悪化することでわかる(1)
・腎動脈の画像検査が有効(1)
・高齢者、糖尿病患者で多い(1)
定義・診断基準(1)
・415の強皮症腎クリーゼに関する論文をレビューした論文(1)によると、強皮症腎クリーゼのゴールドスタンダードはなく、クライテリアは論文ごとにまちまち。以下にそれぞれの論文で使用していた各項目の基準をすべて列挙する。

・高血圧だけでも様々な基準が用いられていることがわかる。稀な疾患なだけにきちんとした定義を定めることが難しいと考えられる
・逆に臨床医としては上記の項目の内いくつかが当てはまる場合は強皮症腎クリーゼを疑って対処すべきとも言える
治療
・ACE阻害薬を用いて72時間以内にBP<140/90mmHgに下げることが目標。例え腎機能が悪化しても許容できる最大用量に増量する。ACE阻害薬の予防的投与はSRC発症をマスクするため、予後不良(2)
・24時間以内にsBP20mmHg、dBP10mmHg低下させることも重要(2)
・ACE阻害薬を最大量に増量しても血圧が下がらない場合はCa拮抗薬(アムロジピン)を第二選択として使用する、第三選択は利尿薬または中枢作動型α拮抗薬(クロニジン)(2)
・低血圧は特にα拮抗薬使用時に注意(2)
・β拮抗薬は腎臓レベルでレイノー現象を悪化させる可能性があるため使用しない(2)
・ARBは単独ではSRCに効果なし(2)
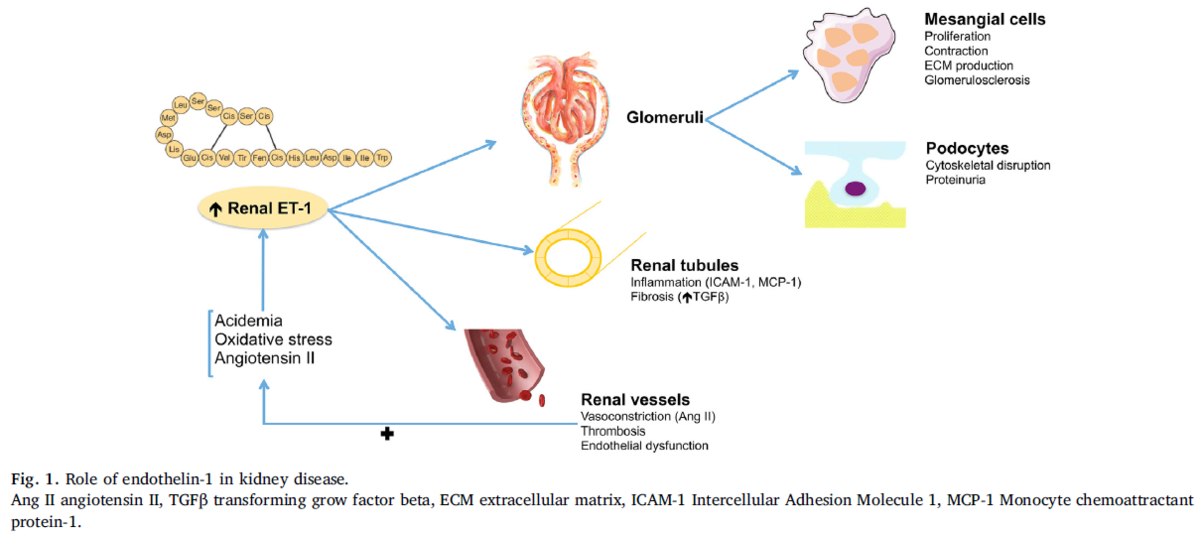
エンドセリン(2)
・エンドセリン-1(ET-1)は血管内皮細胞から産生されるペプチドで血管収縮作用と平滑筋分裂作用を持つ
・ETAとETB受容体があり、両者が活性化すると平滑筋や線維芽細胞が血管収縮を起こす
・さらにTGFβや他の成長因子の転写が促進され、血管リモデリングや線維化が起こる
・ETBのみ刺激はNOやPGI2を介して血管拡張を起こす
・大幅なETAの活性化を介したET-1は腎細胞障害、蛋白尿、炎症、線維化を起こし、CKDとなる
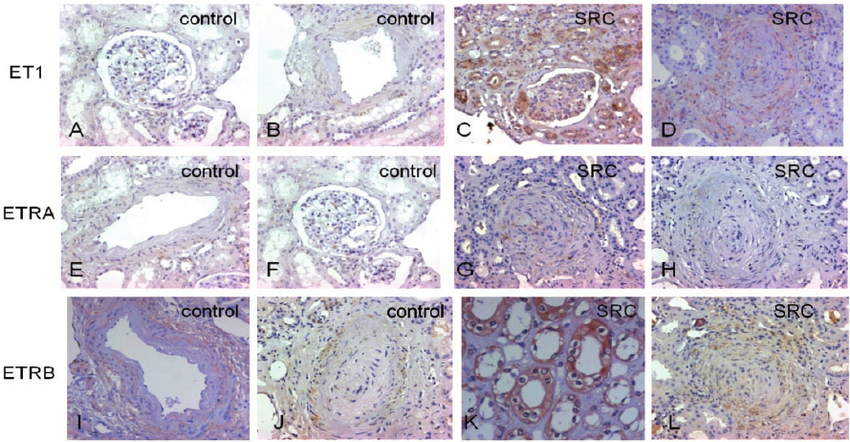
・腎生検組織で糸球体や血管領域でのET-1染色が陽性であることはSRCに特異的という報告も(特にSRC発症1か月以内)
・高用量のエンドセリン受容体拮抗薬(ボセンタン750mg1日2回)が有効であった報告あり
・別の報告ではボセンタン62.5mg1日2回を1か月、その後25mg1日2回を5か月が有効であったという報告あり(3)

エクリズマブ(2)
・高血圧性の剪断ストレスが補体の古典的回路を活性化させる
・SRC患者の腎動脈や糸球体の内皮細胞ではC1q、C3b、C4d、C5b-9の沈着を認めることもある(びまん型>限局型)
・C4dの沈着はSRC患者において腎機能改善不良のリスクを上げる
・血清C3/C4値の低下、C5b-9、C3d/C3比を認める報告もある
・これらはSRCで補体活性化が起こっていることを示している
・C5阻害薬のエクリズマブは溶血や血栓性血小板減少の改善、APSの組織傷害の改善に有効かも
・900mgのエクリズマブ週1回を5週間後、1200mgを2週毎、溶血や血栓性血小板減少がなくなるまで投与
・溶血性微小血管障害が起こっている場合はエクリズマブを投与しても良いかも(補体が活性化されるため)
血漿交換(Plasma exchange: PE)(2)
・SScにおけるPEはET-1のような血管収縮物質、抗核抗体、炎症性・線維化サイトカインを取り除くと考えられている
・SRCに微小血管障害を伴う場合、ACE阻害薬に抵抗性の場合は使用しても良いかも
腎移植(3)
・ほとんどの報告では、12ヵ月後までに腎臓の回復の兆候が見られない場合を除き、透析開始後18〜24ヵ月まではSRC患者の腎移植を遅らせることが推奨されている
予後
・ACE阻害薬を使用すると1年死亡率は15%、無使用の場合は76%(3)
・ただしACE阻害薬を使用していても5年死亡率は50-70%であまり改善していない(2)
・ある145人のSRC患者の報告ではACE阻害薬使用で予後良好であったのは61%(うち透析が不要であったのは38%)、一時透析が必要であったのは23%、38%が予後不良(うち19%が透析で生存し得たが19%は6か月以内に死亡)(3)
・高齢、男性、うっ血性心不全、不十分な血圧コントロール、初期のCre値が3mg/dlより高い時、予後不良(2)
・プレドニゾロンへの暴露は1mg毎に死亡率を4%上げる(2)
・透析が必要でなかったびまん型SScのSRCの予後はSRCでないびまん型SScと同じ(2)
・腎移植後の5年生存率は82.5%でループス腎炎患者と同じ(2)
・NT-proBNPが透析の予測に有用かも、ある報告ではNT-proBNP3373pg/mlで永久的透析、1729pg/mlで一時透析が必要、119pg/mlで透析が不要であったと(3)
・NT-proBNP>1494pg/ml以上では透析が必要(感度87.2%、特異度90.9%)(4)
・レニンとET-1を測定することでSRCの活動性があるかどうか判断できるかも(3)
・SRCの再発率は低い(1.9-2.1%)(3)
【参考文献】
(1) Hoa S. et al. Autoimmun Rev. 2017 Apr;16(4):407-415. Towards developing criteria for scleroderma renal crisis: A scoping review
(2) Zanatta E. et al. Autoimmun Rev. 2018 Sep;17(9):882-889. Therapy of scleroderma renal crisis: State of the art
(3) Woodworth TG. et al. Nat Rev Nephrol. 2016 Nov;12(11):678-691. Scleroderma renal crisis and renal involvement in systemic sclerosis.
(4) Bose N. et al. Semin Arthritis Rheum. 2015 Jun;44(6):687-94. Scleroderma renal crisis.
クリオグロブリン血症 @Lancet2012
Ramos-Casals M. et al. Lancet. 2012 Jan 28;379(9813):348-60. The cryoglobulinaemias.


こちらは日内会誌 100:1289-1295, 2011より引用したものです。

・HCVが肝臓内のB細胞にCB81やLDL受容体を介して感染し、IgG産生が誘導
・B細胞はリウマチ活性を持ったIgM(IgM-RF)も産生する
・HCVのコア蛋白とIgGが結合し、さらにIgM-RFが結合することで免疫複合体が形成される
・この複合体がコア蛋白またはC1qを介して内皮細胞のC1q受容体に結合して血管炎が起こる
・B細胞が産生するIgMのclonal heterogenecityがII型かIII型か決定する
・続いて好中球の動員と補体の活性化が起こる
・さらにマクロファージとTリンパ球も出現する
・最終的にマトリックスメタロプロテアーゼ(MMP)、酸化ストレス分子、TNFαなどのサイトカインが誘導される





・HCV感染がある場合は抗ウイルス薬
・軽症、中等症ではコルチコステロイド併用
・皮膚潰瘍やニューロパチー、腎不全を伴う糸球体腎炎、消化器病変ではコルチコステロイド(0.5-1gのmPSL3日後、1mg/kg/day)にリツキシマブを追加
・致死的な病変がある際には血漿交換、シクロホスファミド(2mg/kg/day経口または750mg/m2/month)またはリツキシマブ追加
・シクロホスファミドの代替薬としてはアザチオプリン2mg/kg/say、ミコフェノール酸モフェチル1g1日おき
・PCPの予防は必須
・血漿交換はクリオグロブリンを取り除くことに優れているが、原疾患の治療は出来ない、中止後に再燃する可能性があるため、シクロホスファミドを併用する
ぶどう膜炎 Uveitis
《眼の解剖》

※ぶどう膜=虹彩+毛様体+脈絡膜
【疫学】
・発生率は17-52人/10万人/年(1)
・有病率は38-714人/10万(1)
・発展途上国の失明の原因の25%に上る(1)
・原因には地域性がある(1)
【遺伝的素因】
・HLA-B27:強直性脊椎炎と関連
・HLA-B29:Birdshot網膜脈絡膜症に関連(99%に陽性となる)
・HLA-B51:ベーチェット病と弱く関連
《日本での発症年齢と男女割合(2)》
 ・男女ともに60歳台にピークがある
・男女ともに60歳台にピークがある
《日本のブドウ膜炎の年代別の発症率の推移(2)》
 ・60歳以上は増加傾向だが、60歳未満は減少傾向、20歳未満は概ね横ばい
・60歳以上は増加傾向だが、60歳未満は減少傾向、20歳未満は概ね横ばい
《ブドウ膜炎の分類(International Uveitis Study Group classification system:SUN)》

因みに前部、中間部、後部、汎ブドウ膜炎を図示すると下記の通りになります(6)

部位別ブドウ膜炎の原因は以下の通り(6)
 ※斜体の原因は頻度が低い
※斜体の原因は頻度が低い
前部ブドウ膜炎
・世界的にはブドウ膜炎の部位別で最多(日本では汎ブドウ膜炎が最多)(1)
・プライマリーケアでは全ぶどう膜炎の90%、専門施設では50-60%(1)
・原因として特発性が最多で38-88%(1)
・原因が特定できたもので最も多いのは脊椎関節症(8-12%)、HLA-B27陽性と関連(1)
・日本で多いのはベーチェット病(9%)(1)
・その他、Fuchs uveitis症候群(1-20%)、ヘルペスブドウ膜炎(1-22%)
サルコイドーシス(1-6%)(1)
・結膜炎と鑑別を要する(結膜炎ではびまん性で充血がややピンク色で眼脂を伴う)(4)
・急性前部ブドウ膜炎の場合、症状は眼痛、充血、羞明(4)
・最も重要な臨床所見は片側前房の細胞増加(4)
・その他、角膜沈着物、後部癒着、虹彩結節(4)
・急性の原因として最も多いのは特発性、その他、強直性脊椎炎も多い(4)
・治療はコルチコステロイド点眼、散瞳薬の点眼(4)
・慢性前部ブドウ膜炎はしばしば無症状、視力低下も起こり得る(4)
・最も重要な臨床所見は両側前房の細胞増加(4)
・慢性の原因として最も多いのは特発性だが、若年性特発性関節炎も多い(4)
・治療は局所コルチコステロイドと散瞳薬に加えて全身の免疫抑制が必要(4)
中間部ブドウ膜炎
・最も少ない部位(全体の15%)(1)
・原因は特発性が最多(60-100%)(1)
・原因を特定できたものではサルコイドーシス、多発性硬化症、
・しばしば両側性(4)
・症状としては飛蚊症、視力低下(嚢胞状黄斑浮腫が視力低下の原因)(4)
・臨床所見として重要なのは周辺部ブドウ膜炎の下部に位置する血管新生を伴う灰白色の血管線維組織のプラーク、その他、硝子体の細胞数増加と靄(4)
・治療は全身の免疫抑制薬(4)
後部ブドウ膜炎
・2番目に多いタイプ(全体の15-30%)(1)
・特発性が最多、その他トキソプラズマ脈絡膜網膜炎(米国、欧米、アフリカではコモン)、CMV、サルコイドーシス、birdspot網膜脈絡膜症、トキソカラ症、急性網膜壊死(1)、結核(4)
・症状は飛蚊症、視力低下、盲点など(4)
・ 臨床所見として重要なのは網膜、脈絡膜の浮腫による視力低下(4)
汎ブドウ膜炎
・南アメリカ、アフリカ、アジアに多い(最多もしくは2番目に多い)(1)
・日本ではVogt-Koyanagi-Harada病、ベーチェット病、サルコイドーシスが多い(他の国では特発性が多い)(1)
《一般的なブドウ膜炎の原因の分類(6)》

《世界のブドウ膜炎の部位別、原因別の頻度(1)》

・非感染では若年性特発性関節炎、外傷、若年性脊椎関節症、ベーチェット病
《日本における原因別頻度(2)》
東京大学病院のブドウ膜炎外来を受診した750名(男性363名、女性387名)の解析



・元来三大原因と言われていたサルコイドーシス、ベーチェット病、原田病を抑えてヘルペスぶどう膜炎が最多となっている、この4つはブドウ膜炎の4大原因
《日本のブドウ膜炎の原因別罹患率の推移(2)》
 ・ヘルペスぶどう膜炎が増加し、元来三大原因とされたサルコイドーシス、ベーチェット病、原田病は低下傾向である
・ヘルペスぶどう膜炎が増加し、元来三大原因とされたサルコイドーシス、ベーチェット病、原田病は低下傾向である
・ヘルペスぶどう膜炎の罹患率が増加しているのはPCRなどの診断法が確立されたためであるが、その他の疾患の罹患率が低下している原因は不明
《日本の4大原因の各国での順位(3)》

・日本で多いサルコイドーシスや原田病はアラビア、イラン、欧州、米国では少ない
・欧州、米国ではベーチェット病は少ない
・上記は2017年の慈恵医大からの報告(3)です。1位がサルコイドーシス、2位が原田病、3位がヘルペス虹彩炎、ベーチェット病となっております。上記の東京大学病院からの報告と比べるとサルコイドーシスの53%以上が臨床診断となっている点、東京大学ではヘルペスぶどう膜炎の6割以上がPCRで診断されていますが、上記報告ではPCRで診断したのが17%である点など、診断方法の違いが順位の誤差を生んだのだと推察されます。
《日本の年代別のブドウ膜炎の原因(2)》



《ブドウ膜炎の発症部位の年代別推移(2)》
 ・前部ブドウ膜炎は減少傾向であるが、汎ブドウ膜炎は増加傾向
・前部ブドウ膜炎は減少傾向であるが、汎ブドウ膜炎は増加傾向
・中間部ブドウ膜炎という概念は後から追加されたため、途中からのデータのみ
【診断】
ブドウ膜炎の原因の頻度を考慮した診断のための3 stepアプローチがあります(5)。

これに参考文献(6)からも少し追加したものを下記に示します(完全の筆者の目線で編集しておりますので、使用時には注意して下さい)。因みに2nd stepからはブドウ膜炎の部位毎の診断アプローチとなるため、眼科医による障害部位の断定が必須です。プライマリケアでは1st stepの検査と問診と診察で前部、中間部、後部ブドウ膜炎のどれかを推定し, 2nd stepの一部まで検査出来れば十分かと思います。なお、赤文字は追試験(7)でさらにより診断に寄与した検査を示したものです。これは意識して行っても良いかもしれません。

【参考文献】
(1) Tsirouki T. et al. Ocul Immunol Inflamm, 26(1), 2–16. A Focus on the Epidemiology of Uveitis.
(2) Shirahama S. et al. BMC Ophthalmol. 2018 Aug 2;18(1):189. Epidemiology of uveitis (2013–2015) and changes in the patterns of uveitis (2004– 2015) in the central Tokyo area: a retrospective study
(3) Takahashi R. et al. Clin Ophthalmol. 2017 Jun 15;11:1151-1156. Uveitis incidence in Jichi Medical University Hospital, Japan, during 2011-2015.
(4) Krishna U. et al. Postgrad Med J. 2017 Dec;93(1106):766-773. Uveitis: a sight-threatening disease which can impact all systems
(5) de Parisot A. et al. Am J Ophthalmol. 2017 Jun;178:176-185. Randomized Controlled Trial Evaluating a Standardized Strategy for Uveitis Etiologic Diagnosis (ULISSE).
(6) Sève P. et al. Autoimmun Rev. 2017 Dec;16(12):1254-1264. Uveitis: Diagnostic work-up. A literature review and recommendations from an expert committee.
(7) Grumet P. et al. Autoimmun Rev. 2018 Apr;17(4):331-343. Contribution of diagnostic tests for the etiological assessment of uveitis, data from the ULISSE study (Uveitis Clinical and medicoeconomic evaluation of a standardized strategy of the etiological diagnosis).
Beers criteria 2019
American Geriatrics Society 2019 Updated AGS Beers Criteria® for Potentially Inappropriate Medication Use in Older Adults.
J Am Geriatr Soc. 2019 Apr;67(4):674-694.
高齢者の約1割は薬剤の副作用のため入院していると言われております(PMID=28251277)。これは外国の報告であり、私の実感では超高齢化社会の日本ではもう少し高い割合のように思います。
高齢者の不要な薬剤を減らそうという『Beers criteria』をご存知の方もおられるかもしれませんが、この度、2019年にUpDateされました。
リウマチ膠原病領域で言えば、ストレス潰瘍予防の過度なPPI処方は避けましょうという点と腎機能障害がある場合のコルヒチンの使用に注意ということでしょうか。
Beers criteria 2019ではH2ブロッカーはむしろ認知症患者で避けるべき薬剤の項目から除外されています。これからは腎機能が良ければPPIよりもH2ブロッカーなのでしょう。
《高齢者に対して潜在的に不適当になり得る薬剤》
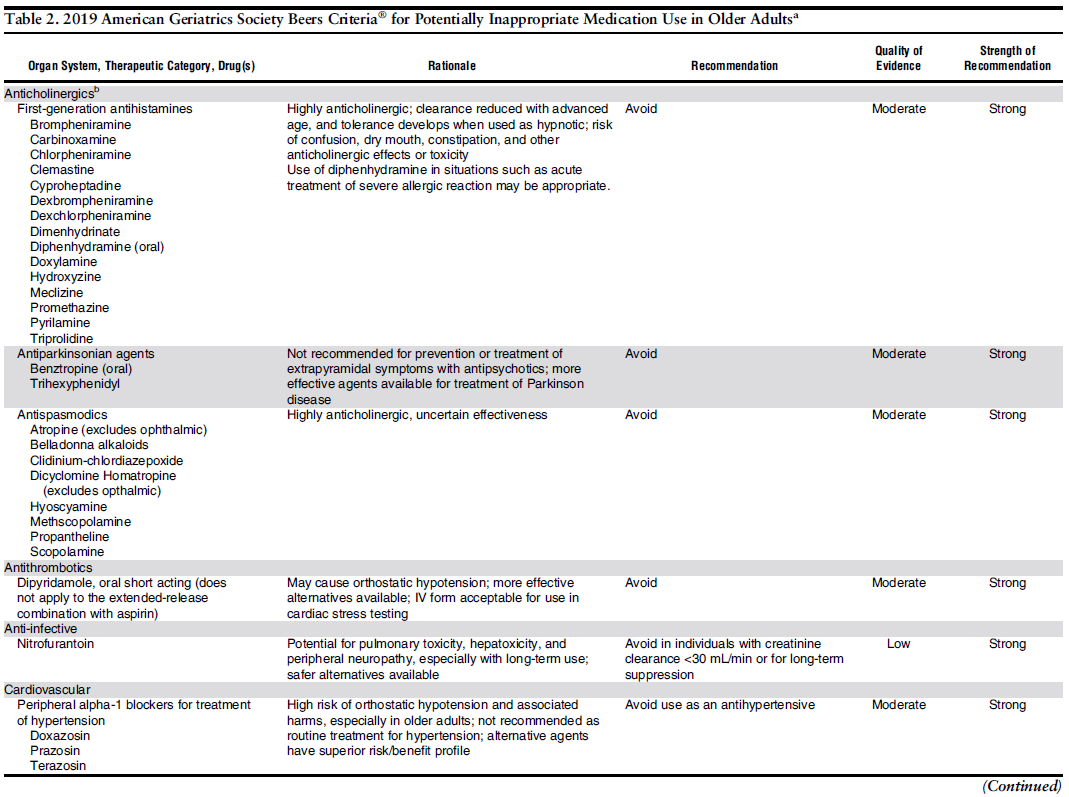


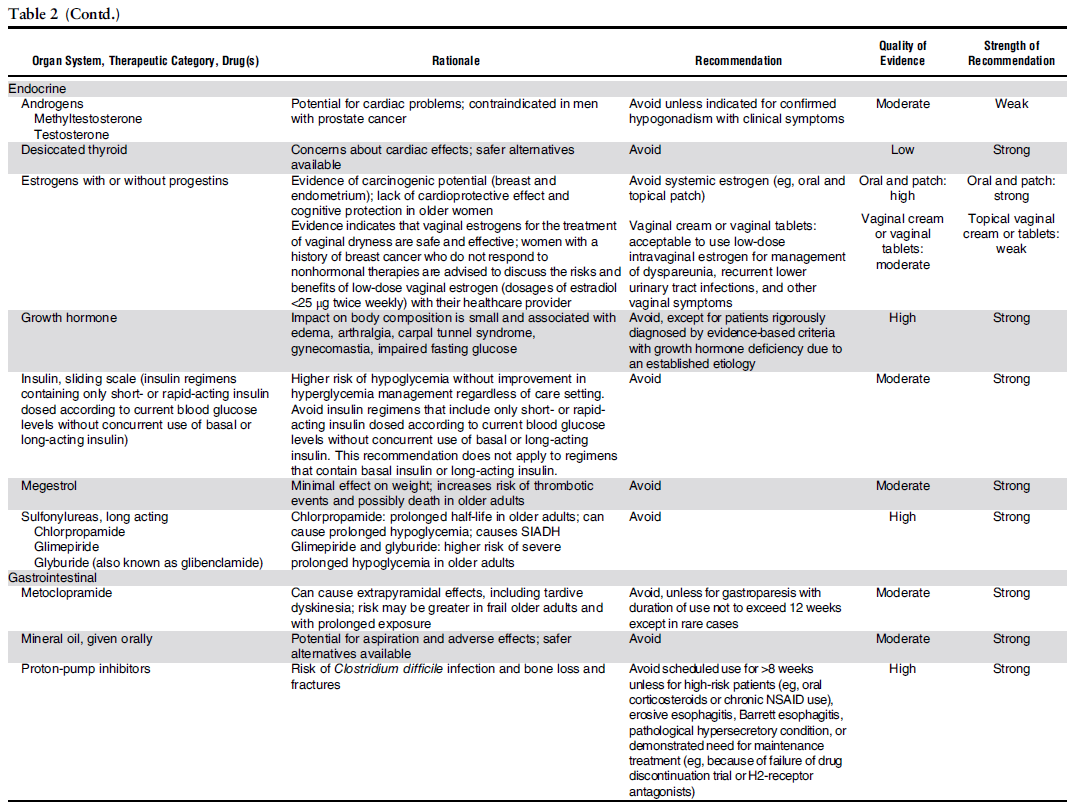
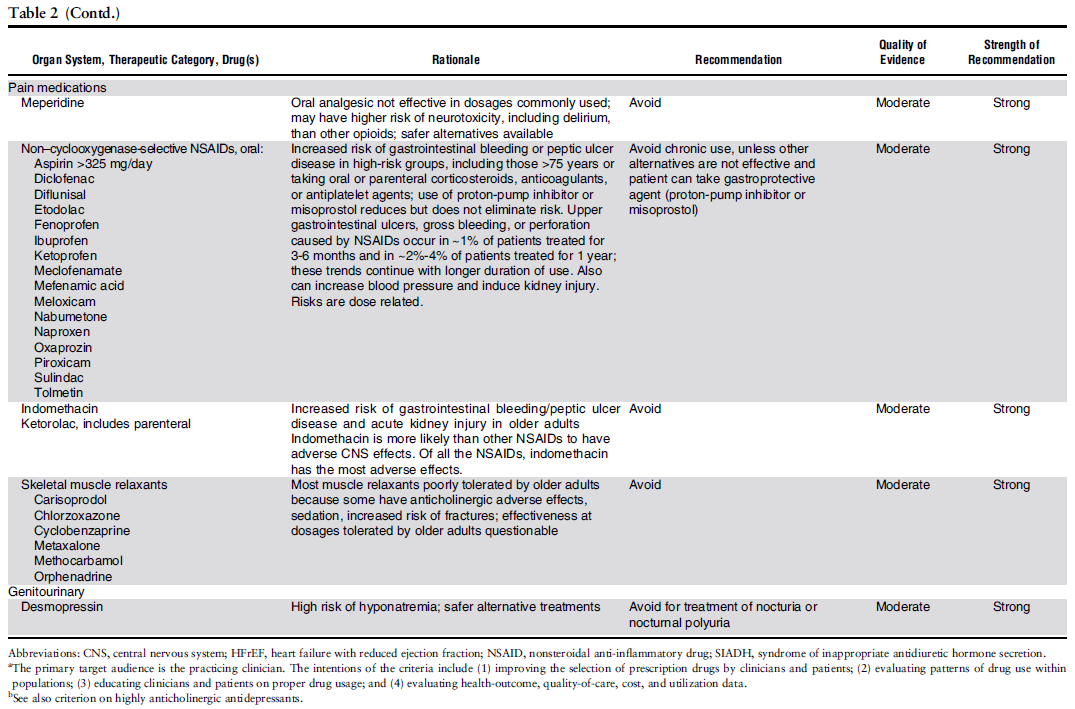
《高齢者の疾患・病態毎の潜在的に不適当となり得る薬剤》



《高齢者に対して潜在的に不適当になり得るため, 使用時に注意すべき薬剤》
《高齢者に対して薬物相互作用の観点から潜在的に不適当になり得る薬剤》
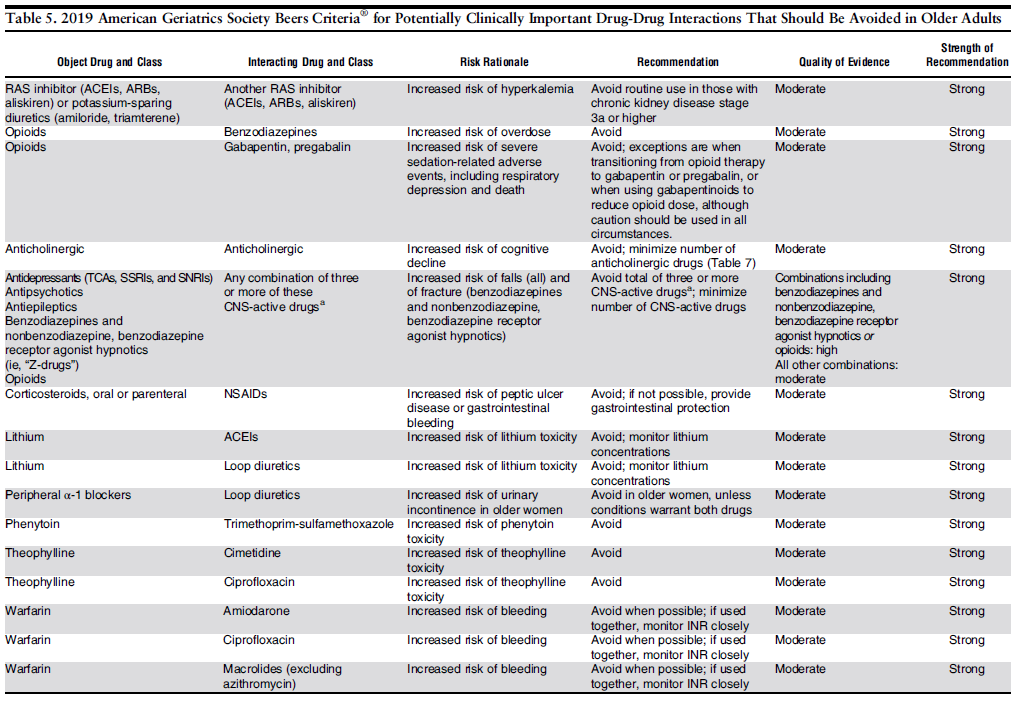
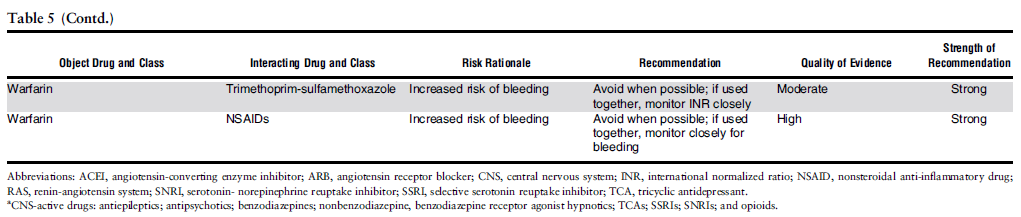
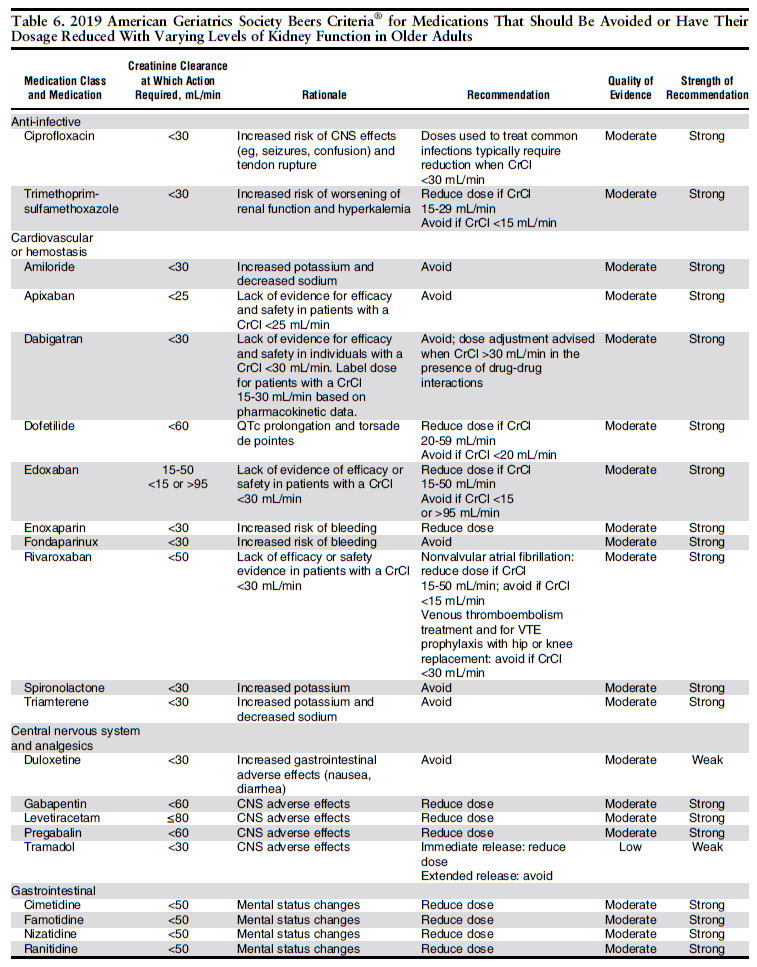
《高齢者に対して腎機能障害のため, 避けるか減量すべき薬剤》

《抗コリン作用を有する薬剤》

《2015年のCriteriaから除外された薬剤》

《2015年のCriteriaに追加された薬剤》

《2015年のCriteriaに変更が加えられた薬剤》

脾臓の石灰化の鑑別
時々CTで見かける『あれ』です。鑑別をまとめました。
ほとんどが静脈結石ですが、肉芽腫性疾患は忘れてはいけません。
Radiopediaから引用しております。

【参考文献】
(1) Tieng AT, Sadow CA, Hochsztein JG et-al. Diffuse calcifications of the spleen: a novel association with systemic lupus erythematosus. Semin. Arthritis Rheum. 2011;41 (2): 187-93.
(2) Vanhoenacker FM, Van den brande P, De schepper AM. Hepatosplenic antracosilicosis: a rare cause of splenic calcifications. Eur Radiol. 2001;11 (7): 1184-
(3) Moody AR, King DM. Splenic calcification following treatment of Hodgkin's disease. Br J Radiol. 1991;64 (757): 55-6.
(4) Gibson JM, Baillod R, Platts AD. Hepatic and splenic calcification due to amyloidosis. Clin Radiol. 1992;45 (1): 68.
(5) Kennan NM, Evans C. Case report: hepatic and splenic calcification due to amyloid. Clin Radiol. 1991;44 (1): 60-1.
(6) Burgener FA, Kormano M, Pudas T. Differential Diagnosis in Conventional Radiology. Thieme Medical Pub. (2007) ISBN:1588902757
(7) Fyfe AJ, Gallipoli P. Multiple splenic calcifications. Br. J. Haematol. 2009;144 (6): 808
(8) Talenti E, Cesaro S, Scapinello A et-al. Disseminated hepatic and splenic calcifications following cat-scratch disease. Pediatr Radiol. 1995;24 (5): 342-3.
(9) Thomas Benter. Sonography of the Spleen. JUM. 2011;30 (9): 1281-1293.
(10) Wolfgang Dähnert. Radiology Review Manual. (2011)
(11) Wolfgang Dähnert. Radiology Review Manual. (2011)
(12) A Nakao, S Saito, T Yamano, et al. Dermoid cyst of the spleen: Report of a case. (1999) Surgery Today. 29 (7): 660.