強皮症腎クリーゼ Scleroderma renal crisis(SRC)
概念
・強皮症(Systemic Sclerosis: SSc)は血管障害や線維化によって皮膚硬化がや臓器障害が引き起こされることが特徴的な自己免疫性疾患(1)
・強皮症腎クリーゼ(Scleroderma renal crisis: SRC)は稀な強皮症の合併症(1)
・新規発症で急速進行性の腎動脈性高血圧、急速進行性乏尿性腎機能障害、中等度の血圧上昇と腎機能障害、正常血圧など様々な臨床スペクトラムを有する(1)
・SRCが強皮症の初期症状となることもあり得る(3)
・正常血圧SRCの1/4が強皮症の診断なく、SRCが初発症状となる(4)
疫学
・全強皮症では5-13%(1)
・びまん型では11-20%(1)(2)、限局型では4%(1)
・頻度はどんどん下がっていると(2)
・これはレイノー現象に対する血管拡張薬の使用が広がったためと、SRCのリスクとなるため、コルチコステロイドの使用が慎重となったためと考えられる(2)
・高血圧が主だが、正常血圧は10%に起こり、予後不良(2)
・溶血性微小血管障害は50%に起こる(2)
病態
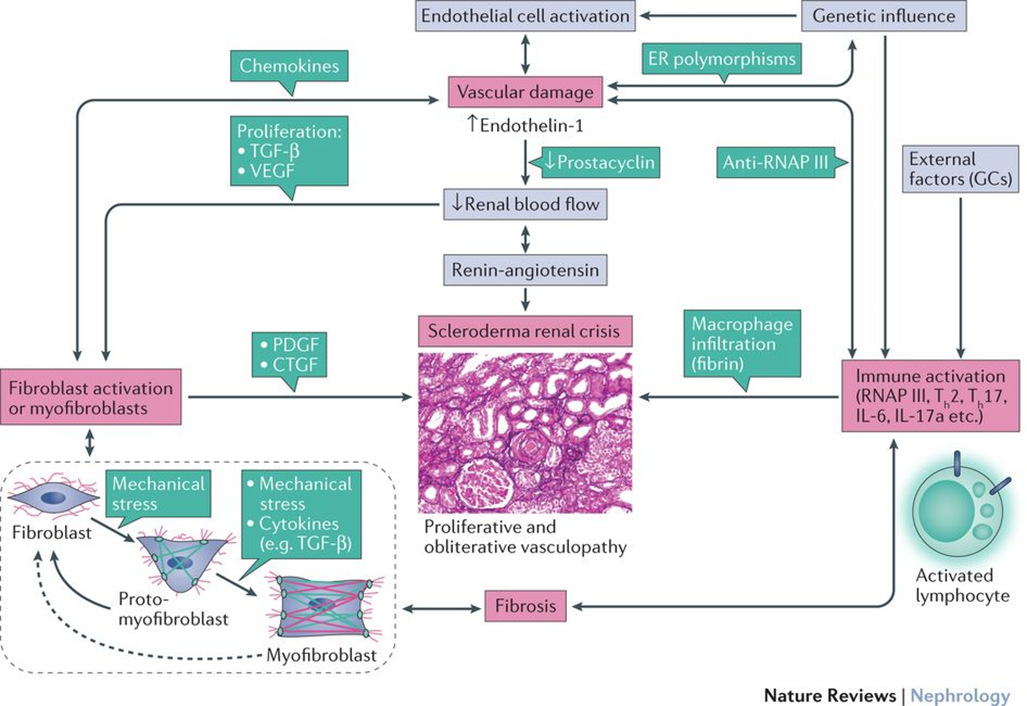
※下記表は文献(3)から

※下記表は文献(4)から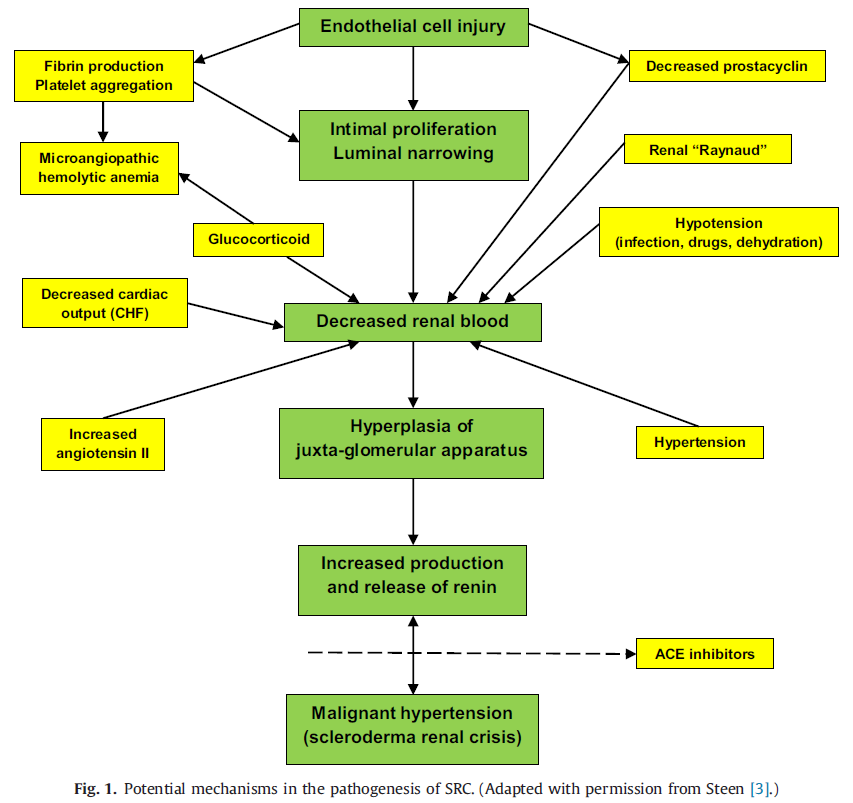
・明確に理解されているわけではないが、微小血管の内皮細胞障害が起こり、血管透過性が亢進することで内皮細胞の増殖、フィブリノイド血栓を伴う血小板凝集が起こる(2)
・これにより小葉間や球状腎動脈の内膜肥厚と線維化領域を伴う増殖性閉塞性血管症が起こる(Onion skin lesions)(2)
・腎血流が低下すると糸球体虚血が起こり、レニン-アンギオテンシン系が活性化し、重篤な腎動脈性高血圧を起こす(2)
・一方で狭窄した同部位では塞栓性微小血管障害や溶血性貧血が起こり、末梢血に破砕赤血球が出現する(2)
・この糸球体病変は非炎症性で免疫沈着物も認めない(2)
病理(3)
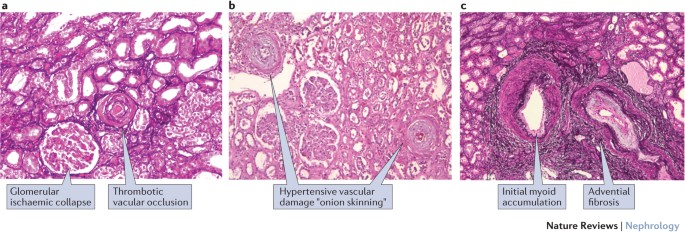

・a: 高血圧性血管障害, 血栓性血管閉塞, 糸球体の虚血性荒廃, びまん性尿細管変性
・b: Onion skin lesions
・c: 内膜の筋組織蓄積と外膜の線維化
リスク因子(1)
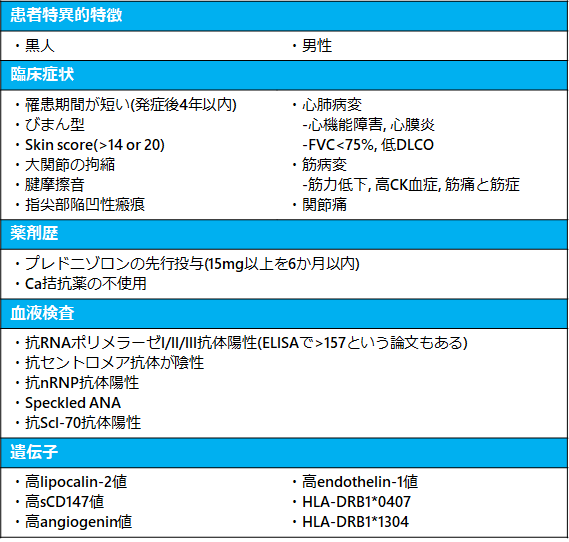
※sCD147: 細胞外マトリックスメタロプロテアーゼ阻害因子
・SRCの75%が強皮症発症(レイノー現象を除く症状)4年以内(2)
・1年間で急速に皮膚硬化が起こる場合もリスク(2)
・mRSSがSRC発症前の6か月間で、50%の患者で上昇したという(2)
・心拡大やうっ血性心不全は腎血流低下を起こし、SRCの潜在的なリスクとなり得る(2)
鑑別(1)
・ANCA関連糸球体腎炎(37%)
・TTP/HUS(21%)
・膜性腎症(7%)
・膜性増殖性糸球体腎炎(1%)
・その他の血管炎(結節性多発動脈炎、混合型クリオグロブリン血症、Goodpasture症候群)(7%)
・薬剤性腎症(D-ペニシラミン、シクロスポリンなど)(5%)
・シュウ酸腎症(4%)
・腎動脈狭窄(4%)
・腎前性(敗血症、脱水症)(1%)
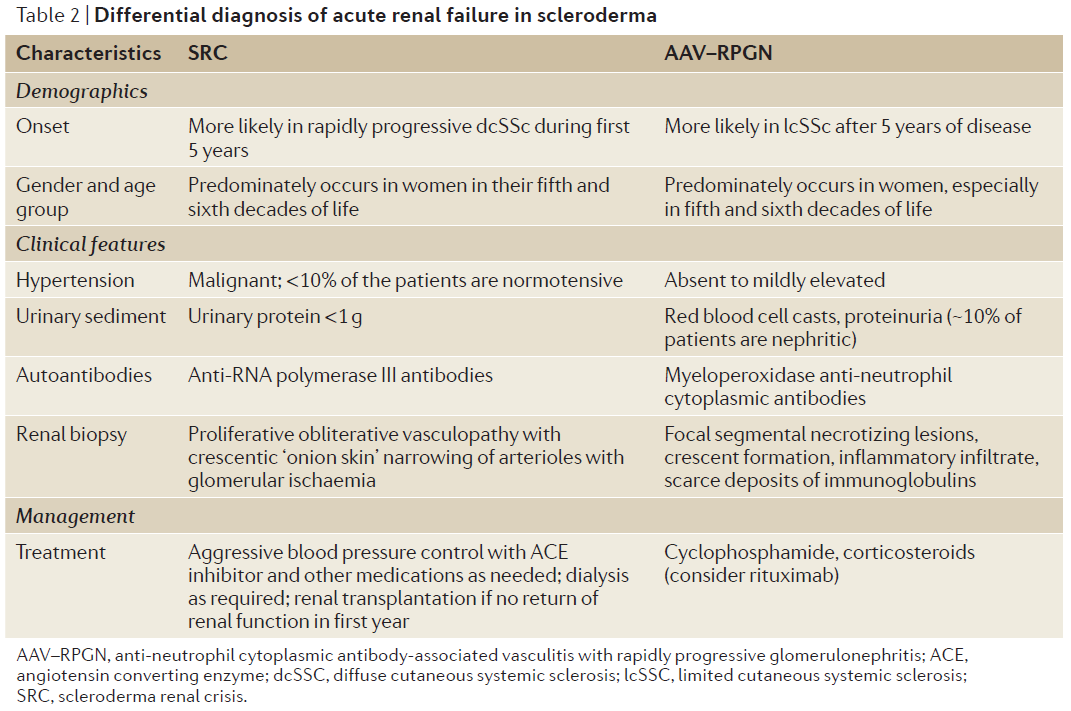
ANCA関連糸球体腎炎
・特にMPO-ANCAが95%以上に見られる(1)
・pauci-immune壊死性、半月体形成性糸球体腎炎が腎生検で見られる(1)
・その他、肺胞出血や皮疹、手指虚血などの血管炎症状を認める(1)
・免疫抑制療法が有用なのはSRCと異なる(1)
・すべてのタイプのSSc(限局型から強皮症症状のないSScまで)に合併し(59%)(1)、抗Scl-70抗体陽性(77%)、SScの罹患期間が長い(8±7.7年)(1)
・正常血圧が多い(sBP<160mmHg)(82%)、MAHAやTTP、高レニン血漿を伴わない(1)
・別の報告ではRPGNを伴うAAVは限局型SScの晩期、Overlap症候群、稀に混合型クリオグロブリン血症に見られるという(3)
・診断が不明な時は腎生検を行う(3)
・無症状の時のANCA陽性は意味がない(SScでは0-11.7%でANCA陽性となる)(3)
※以下の図は論文(3)より引用
TTP
・抗ADAMTS-13抗体を伴うADAMTS-13活性の欠損、重篤な血小板減少(特に<5万/μl)、出血合併症(紫斑、消化管出血)、発熱、血漿交換が著効することなどはSRCよりもTTPを指示する所見(1)
・正常血圧が多く、限局型、長期罹患患者に多い(1)
・腎生検では原発性糸球体毛細血管の微小血管障害を認めるが、SRCでは糸球体外微小血管病変を有する点が異なる(1)
シュウ酸腎症
・脂肪吸収不良や抗菌薬が必要なSIBOを起こすほどの重篤な消化器病変を有する場合に疑う(1)
・正常血圧が多く、溶血や尿検査異常を伴わない(1)
・シュウ酸結晶は尿検査で認め、24時間蓄尿でシュウ酸の増加を認める(1)
・腎生検ではびまん性尿細管内の複屈曲性結晶を含むカルシウム沈着物を認める(1)
腎動脈狭窄
・ACE阻害薬を使用すると腎機能障害が悪化することでわかる(1)
・腎動脈の画像検査が有効(1)
・高齢者、糖尿病患者で多い(1)
定義・診断基準(1)
・415の強皮症腎クリーゼに関する論文をレビューした論文(1)によると、強皮症腎クリーゼのゴールドスタンダードはなく、クライテリアは論文ごとにまちまち。以下にそれぞれの論文で使用していた各項目の基準をすべて列挙する。

・高血圧だけでも様々な基準が用いられていることがわかる。稀な疾患なだけにきちんとした定義を定めることが難しいと考えられる
・逆に臨床医としては上記の項目の内いくつかが当てはまる場合は強皮症腎クリーゼを疑って対処すべきとも言える
治療
・ACE阻害薬を用いて72時間以内にBP<140/90mmHgに下げることが目標。例え腎機能が悪化しても許容できる最大用量に増量する。ACE阻害薬の予防的投与はSRC発症をマスクするため、予後不良(2)
・24時間以内にsBP20mmHg、dBP10mmHg低下させることも重要(2)
・ACE阻害薬を最大量に増量しても血圧が下がらない場合はCa拮抗薬(アムロジピン)を第二選択として使用する、第三選択は利尿薬または中枢作動型α拮抗薬(クロニジン)(2)
・低血圧は特にα拮抗薬使用時に注意(2)
・β拮抗薬は腎臓レベルでレイノー現象を悪化させる可能性があるため使用しない(2)
・ARBは単独ではSRCに効果なし(2)
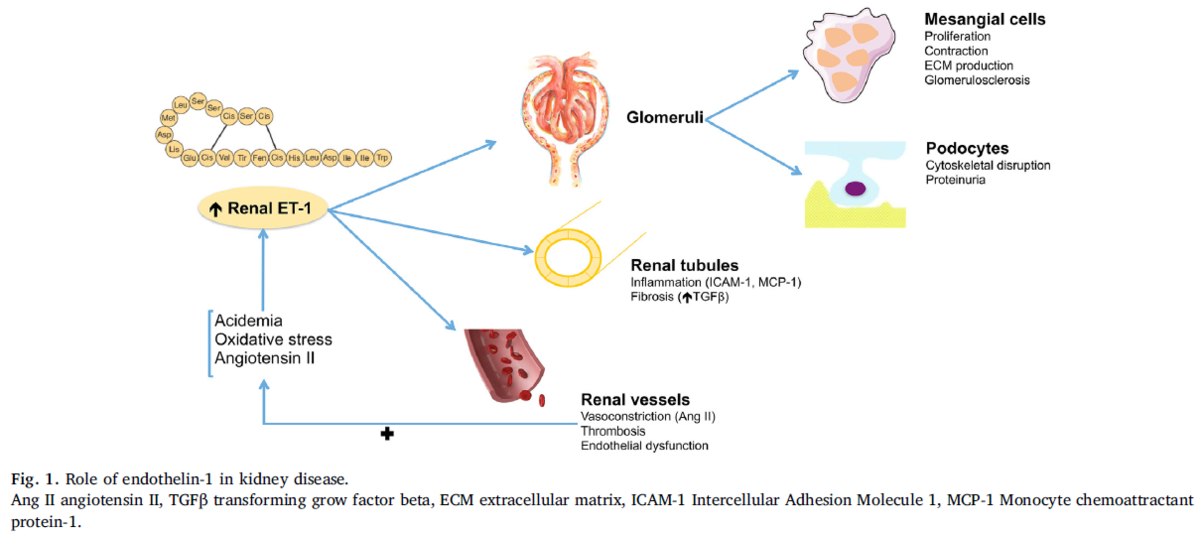
エンドセリン(2)
・エンドセリン-1(ET-1)は血管内皮細胞から産生されるペプチドで血管収縮作用と平滑筋分裂作用を持つ
・ETAとETB受容体があり、両者が活性化すると平滑筋や線維芽細胞が血管収縮を起こす
・さらにTGFβや他の成長因子の転写が促進され、血管リモデリングや線維化が起こる
・ETBのみ刺激はNOやPGI2を介して血管拡張を起こす
・大幅なETAの活性化を介したET-1は腎細胞障害、蛋白尿、炎症、線維化を起こし、CKDとなる
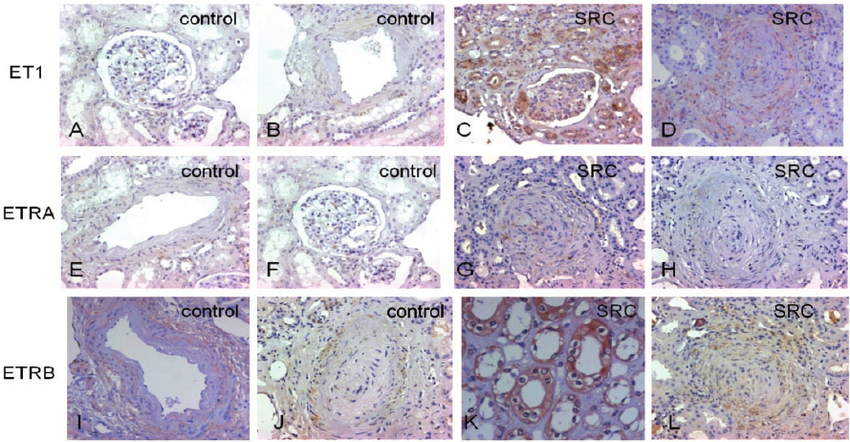
・腎生検組織で糸球体や血管領域でのET-1染色が陽性であることはSRCに特異的という報告も(特にSRC発症1か月以内)
・高用量のエンドセリン受容体拮抗薬(ボセンタン750mg1日2回)が有効であった報告あり
・別の報告ではボセンタン62.5mg1日2回を1か月、その後25mg1日2回を5か月が有効であったという報告あり(3)

エクリズマブ(2)
・高血圧性の剪断ストレスが補体の古典的回路を活性化させる
・SRC患者の腎動脈や糸球体の内皮細胞ではC1q、C3b、C4d、C5b-9の沈着を認めることもある(びまん型>限局型)
・C4dの沈着はSRC患者において腎機能改善不良のリスクを上げる
・血清C3/C4値の低下、C5b-9、C3d/C3比を認める報告もある
・これらはSRCで補体活性化が起こっていることを示している
・C5阻害薬のエクリズマブは溶血や血栓性血小板減少の改善、APSの組織傷害の改善に有効かも
・900mgのエクリズマブ週1回を5週間後、1200mgを2週毎、溶血や血栓性血小板減少がなくなるまで投与
・溶血性微小血管障害が起こっている場合はエクリズマブを投与しても良いかも(補体が活性化されるため)
血漿交換(Plasma exchange: PE)(2)
・SScにおけるPEはET-1のような血管収縮物質、抗核抗体、炎症性・線維化サイトカインを取り除くと考えられている
・SRCに微小血管障害を伴う場合、ACE阻害薬に抵抗性の場合は使用しても良いかも
腎移植(3)
・ほとんどの報告では、12ヵ月後までに腎臓の回復の兆候が見られない場合を除き、透析開始後18〜24ヵ月まではSRC患者の腎移植を遅らせることが推奨されている
予後
・ACE阻害薬を使用すると1年死亡率は15%、無使用の場合は76%(3)
・ただしACE阻害薬を使用していても5年死亡率は50-70%であまり改善していない(2)
・ある145人のSRC患者の報告ではACE阻害薬使用で予後良好であったのは61%(うち透析が不要であったのは38%)、一時透析が必要であったのは23%、38%が予後不良(うち19%が透析で生存し得たが19%は6か月以内に死亡)(3)
・高齢、男性、うっ血性心不全、不十分な血圧コントロール、初期のCre値が3mg/dlより高い時、予後不良(2)
・プレドニゾロンへの暴露は1mg毎に死亡率を4%上げる(2)
・透析が必要でなかったびまん型SScのSRCの予後はSRCでないびまん型SScと同じ(2)
・腎移植後の5年生存率は82.5%でループス腎炎患者と同じ(2)
・NT-proBNPが透析の予測に有用かも、ある報告ではNT-proBNP3373pg/mlで永久的透析、1729pg/mlで一時透析が必要、119pg/mlで透析が不要であったと(3)
・NT-proBNP>1494pg/ml以上では透析が必要(感度87.2%、特異度90.9%)(4)
・レニンとET-1を測定することでSRCの活動性があるかどうか判断できるかも(3)
・SRCの再発率は低い(1.9-2.1%)(3)
【参考文献】
(1) Hoa S. et al. Autoimmun Rev. 2017 Apr;16(4):407-415. Towards developing criteria for scleroderma renal crisis: A scoping review
(2) Zanatta E. et al. Autoimmun Rev. 2018 Sep;17(9):882-889. Therapy of scleroderma renal crisis: State of the art
(3) Woodworth TG. et al. Nat Rev Nephrol. 2016 Nov;12(11):678-691. Scleroderma renal crisis and renal involvement in systemic sclerosis.
(4) Bose N. et al. Semin Arthritis Rheum. 2015 Jun;44(6):687-94. Scleroderma renal crisis.