クリオグロブリン血症 @Lancet2012
Ramos-Casals M. et al. Lancet. 2012 Jan 28;379(9813):348-60. The cryoglobulinaemias.
【ポイント】
・3タイプあるが、重要なのはモノクローナルガンマパチーがすべてを占めるI型かその他の混合型(II型、III型)かどうかを分ける
・混合型ではC型肝炎が最多、その他自己免疫疾患(シェーグレン症候群など)を検索
・沈殿したクリオグロブリン自体を免疫固定法などで判定する方法もあるがコマーシャルベースでは無理そう
・多くは無症状だが、I型ではクリオグロブリンが大量のため、微小血管に詰まることで起こる過粘稠度症候群による血流障害が問題、混合型(特にII型)ではクリオグロブリンと補体などの免疫複合体が血管炎(クリオグロブリン血管炎)を起こすことが問題
・クリオグロブリン血管炎の症状は主に皮膚、神経、腎臓
・皮膚症状は紫斑が多く、網状皮斑、潰瘍、レイノー現象など、下肢に多い
・腎病変は無症候性蛋白尿、尿潜血が半数、病理は膜性増殖性糸球体腎炎
・神経症状は下肢優位の感覚障害、夜間の灼熱感など
・治療はタイプによって異なる、I型ではリンパ増殖疾患の化学療法(リツキシマブ)など
・混合型で血管炎を起こした場合はステロイド+シクロホスファミドなどの血管炎治療
・最重症型では血漿交換も併用
《定義と分類》
・3タイプあり
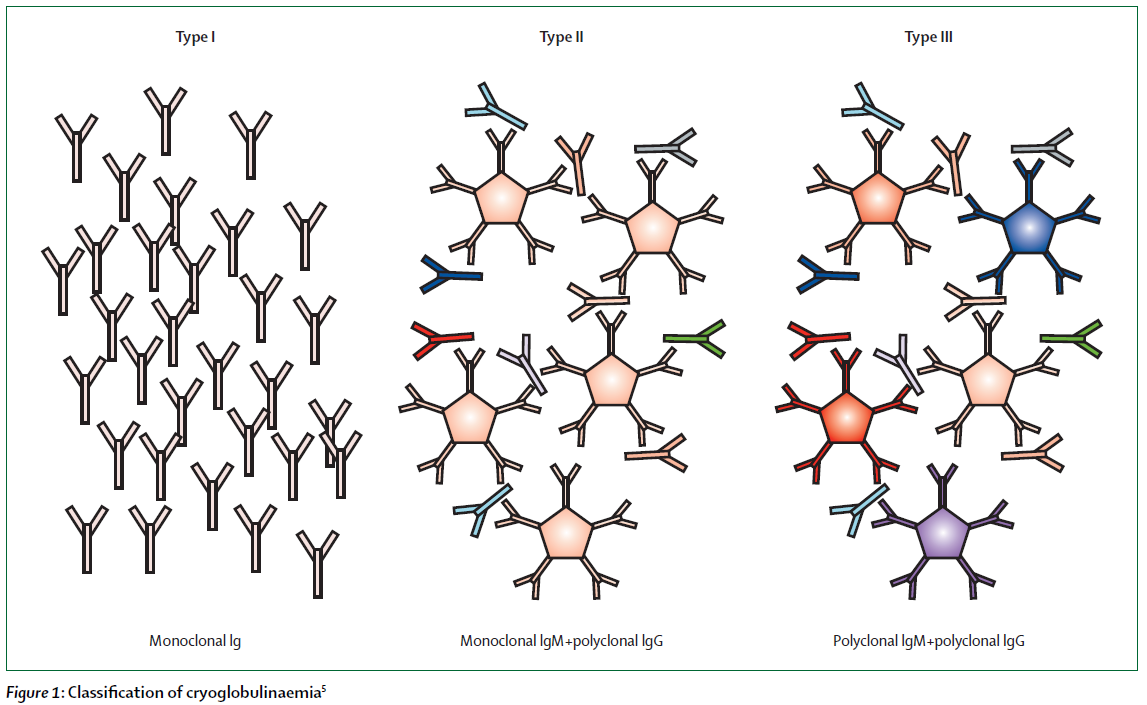
Type I(10-15%):単クローン性IgMまたはIgG
Type II(50-60%):単クローン性IgM(RFの働きがある)と多クローン性IgG
Type III(30-40%):多クローン性IgMとIgG
・Type IIとType IIIは混合型クリオグロブリン血症とも言う
※Type IIIはType IIへ移行する過渡期と主張する研究者も
《原因》
・自己免疫:シェーグレン症候群が最多(腺外症状、B細胞リンパ腫、予後不良と関連)
・悪性腫瘍:B細胞リンパ腫(混合型クリオグロブリン血症)
・I型はほとんどがモノクローナルガンマパチーを起こす疾患(MGUSや多発性骨髄腫)
・II型はHCV関連がほとんど、その他、自己免疫疾患(シェーグレン症候群 etc)
・III型はB細胞リンパ腫、HBV関連、自己免疫疾患(シェーグレン症候群 etc)
・III型クリオグロブリン血症の10%は特発性

《疫学》
・地中海に多い
・HCV罹患年数に関係(年間3%ずつリスクがあがる)

こちらは日内会誌 100:1289-1295, 2011より引用したものです。

・HCVが肝臓内のB細胞にCB81やLDL受容体を介して感染し、IgG産生が誘導
・B細胞はリウマチ活性を持ったIgM(IgM-RF)も産生する
・HCVのコア蛋白とIgGが結合し、さらにIgM-RFが結合することで免疫複合体が形成される
・この複合体がコア蛋白またはC1qを介して内皮細胞のC1q受容体に結合して血管炎が起こる
・B細胞が産生するIgMのclonal heterogenecityがII型かIII型か決定する
・続いて好中球の動員と補体の活性化が起こる
・さらにマクロファージとTリンパ球も出現する
・最終的にマトリックスメタロプロテアーゼ(MMP)、酸化ストレス分子、TNFαなどのサイトカインが誘導される
《病理》
・クリオグロブリンはB細胞から産生される
・Typ IとType IIは単クローン性(MMやWaldenstrom's macroglobulinaemia, 形質細胞腫, リンパ腫)
・Type IIIは多クローン性
・この相互作用がB細胞刺激を引き起こす
・低温でクリオグロブリンが析出する機序はわかっていない上、低温だけが因子ではなさそう(四肢は低温環境であるため、血管障害の原因因子として低温は説明できるが、内臓は恒温環境であるため、低温だけが原因として説明できない)
・蛋白質の溶解性が関係するかも(初期の構造、温度やpHなどに応じて起こる立体構造変化)
《組織障害機序》
②免疫複合体介在性炎症:混合型(特にType II)に多い、単クローン性IgMがIgGやC1qなどの補体と巨大な免疫複合体を形成、C1qが血管内皮の受容体に結合し、免疫複合体が血管内へ沈着し血管炎症を引き起こす
《症状》
・多くは無症状
・有症状は2-50%
・3徴候は紫斑、関節痛、脱力で初発症状の80%
過粘稠度症候群
・I型が主(混合型は3%未満)
・神経症状(頭痛、混乱)、視覚症状(霧視、視力低下)、聴覚症状(鼻出血、聴力低下)、腎機能障害
・血液の粘稠度が診断有用
・症候性の過粘稠状態は血漿交換などの緊急的な治療が必要
クリオグロブリン血管炎
・発熱、関節痛(手、手首、膝など(44-71%)、炎症所見はない)、筋肉痛、脱力など
・関節炎は10%未満、骨びらんなし、ACPA陰性(関節リウマチに合併する例では例外)
・皮疹では紫斑が最も特徴的(54-82%、腹部までは出るが、胸部や上肢は少ない)
・水疱性病変は稀
・紫斑は1週間以内に自然寛解することもあるが、運動や脱毛で誘発される
・網状皮斑(Livedo reticularis)や皮膚潰瘍は中血管病変を示唆
・20%は診断時に腎機能障害を呈し、30%は経過中に腎合併症を呈する
・半分の患者で蛋白尿、尿潜血、赤血球円柱、様々な程度の腎機能障害を呈する
・ネフローゼ症候群は21%、糸球体腎炎は14%
・70%以上が高血圧を持ち、40-60%に診断時に血清Cre値の上昇(>1.5mg/dl)を認める
・17-60%が末梢神経障害(感覚障害)を呈し、初期症状となり得る
・神経症状は下肢に多い、夜間に増悪する灼熱感
・神経伝導検査ではポリニューロパチー
・2-6%に消化器症状(小腸虚血など)
・腸管虚血の1/3に発熱、血便を認める
・胆嚢炎や膵炎と同じような症状を起こすこともある
・肺病変は5%未満(肺線維症、肺胞出血、胸水など)
・CNS病変は6%(脳卒中が最多、他、脳症、横断性脊髄炎、脊髄梗塞など)
・心筋血管炎は10例未満の報告


《診断》
クリオグロブリン試験
・37度以上に温めたシリンジで血液検査を行う、移送中も37-40度に保つ
・その後4度で7日間まで保管する
・Type Iクリオグロブリンは数時間で沈殿する
・混合型(特にType III)は沈殿するのに数日かかる
・健常者でも低濃度(0.06g/L未満)のクリオグロブリンを有する
・血清クリオプロテイン量は過粘稠度症候群において重症度と治療モニタリングに有用
Laboratory test
・低補体(特にC4)とRF値上昇は混合型クリオグロブリンにしばしば認められる
組織学的
・血管炎は混合型クリオグロブリン血症の特徴だが、小血管にフィブリノイド壊死が起こる(皮膚、腎、末梢神経で認める)
・紫斑部の皮膚生検では白血球破砕性血管炎を認める
・半月体形成は10-20%、腎壊死性血管炎は5-30%、間質性腎炎は稀
・神経障害は末梢血管や神経内血管の血管炎による
・軸索変性や脱ミエリンなどが起こる
・神経内血管病変は他の血管炎よりもよく見られる
・神経内血管は肥厚し、血管外に赤血球やマクロファージが漏出する

《予後》
・半数近い患者が致死的臓器でない慢性疾患を背景に持つ
・1/3の患者は中等度から重症の疾患を背景に持つ(腎不全や肝硬変)
・155が致死的疾患を背景に持つ
・10年生存率は低い
致死的なクリオグロブリン血症
・糸球体腎炎は10%が急性腎不全となり、慢性腎不全に移行する
・10年生存率は33-49%(一部80%という報告もあるが)
・腸管虚血や肺胞出血の致死率も高い(80%以上)
悪性腫瘍のリスク
・B細胞性リンパ腫は混合型(II型、III型)の5-22%に見られる
・低ガンマグロブリン血症はリンパ腫形成の指標になり得る
・HCV感染はB細胞性リンパ腫のリスクを20-30%上げる
・B細胞性リンパ腫はクリオグロブリン血症の診断後10年以内に起こる
・びまん性、大細胞性、結節辺縁系、リンパ形質細胞性リンパ腫などが起こる
《治療》


・HCV感染がある場合は抗ウイルス薬
・軽症、中等症ではコルチコステロイド併用
・皮膚潰瘍やニューロパチー、腎不全を伴う糸球体腎炎、消化器病変ではコルチコステロイド(0.5-1gのmPSL3日後、1mg/kg/day)にリツキシマブを追加
・致死的な病変がある際には血漿交換、シクロホスファミド(2mg/kg/day経口または750mg/m2/month)またはリツキシマブ追加
・シクロホスファミドの代替薬としてはアザチオプリン2mg/kg/say、ミコフェノール酸モフェチル1g1日おき
・PCPの予防は必須
・血漿交換はクリオグロブリンを取り除くことに優れているが、原疾患の治療は出来ない、中止後に再燃する可能性があるため、シクロホスファミドを併用する